Eine neue Forschungsrichtung legt nahe, dass die menschliche Fruchtbarkeit von komplexen immunologischen Mechanismen abhängt, die bis vor Kurzem in der konventionellen Medizin kaum erforscht wurden.
Sollte sich diese Dimension bestätigen, könnte Unfruchtbarkeit nicht mehr nur als hormonelles oder anatomisches Problem betrachtet werden, sondern als eine Frage der Immunregulation.
Von Ehab Soltan
HoyLunes — Über Jahrzehnte hinweg wurde Unfruchtbarkeit primär durch drei Prismen analysiert: das hormonelle, das anatomische und das genetische. Die Suche konzentrierte sich auf verschlossene Eileiter, Ovulationsstörungen oder Chromosomenanomalien. Doch trotz fortschrittlichster Diagnosetechnik stehen Mediziner weltweit oft vor einem Rätsel: der „idiopathischen Sterilität“ – der Unfähigkeit zur Empfängnis ohne erkennbare Ursache.
Das Ausmaß des Problems rechtfertigt das wachsende wissenschaftliche Interesse. Nach Angaben der Weltgesundheitsorganisation (WHO) ist jeder sechste Mensch weltweit irgendwann in seinem Leben von Unfruchtbarkeit betroffen. Beunruhigend ist, dass Spezialisten in einem signifikanten Prozentsatz — zwischen 10 % und 30 % der Fälle — keine klare medizinische Erklärung finden. Dieses diagnostische Vakuum hat eine provokante Frage aufgeworfen: Was wäre, wenn ein wesentlicher Teil dieser Fälle in Wirklichkeit eine unerkannte immunologische Störung wäre?
Unser Immunsystem ist weit mehr als eine Abwehrtruppe gegen Krankheitserreger. Es fungiert als hochempfindlicher Regulator biologischer Prozesse, bei denen die Schwangerschaft das ehrgeizigste „diplomatische Projekt“ der Natur darstellt. Eine harmonische Interaktion zwischen dem mütterlichen Organismus und dem Embryo ist kein Zufallsprodukt, sondern das Ergebnis subtiler molekularer Verhandlungen.

Die Schwangerschaft: Eine außergewöhnliche immunologische Herausforderung
Aus der Perspektive der klassischen Immunologie ist eine Schwangerschaft ein Paradoxon. Der Embryo trägt die genetische Signatur des Vaters, was ihn zu einem „Semiallotransplantat“ macht: ein Gewebe, das für den mütterlichen Körper zu 50 % fremd ist.
Normalerweise würde das Immunsystem jede Zelle eliminieren, die nicht als „eigen“ identifiziert wird. Während der Gestation geschieht jedoch das Wunder der mütterlich-fetalen Immuntoleranz. Die Mutter muss den Embryo nicht nur tolerieren, sondern ihn aktiv unterstützen, ohne ihre Wachsamkeit gegenüber tatsächlichen Infektionen zu verringern. Wenn diese „Diplomatie“ scheitert, beginnt der Körper, den Gast als Eindringling zu behandeln.
Während der Implantation durchläuft das Immunsystem eine bemerkenswerte Reorganisation. Einige Zellen reduzieren ihre zytotoxische Aktivität (Angriff), während andere regulatorische Funktionen übernehmen. Dieser Prozess beinhaltet molekulare Interaktionen zwischen dem Endometrium und dem Embryo, die heute im Zentrum der Forschung an den weltweit fortschrittlichsten Reproduktionszentren stehen.
Wenn das Immunsystem zum Hindernis wird
Untersuchungen zeigen, dass immunologische Dissonanzen den Fortpflanzungsprozess in kritischen Phasen sabotieren können:
Fehlgeschlagene Einnistung (Implantation): Ungleichgewichte, die den für die Einnistung des Embryos notwendigen initialen „Dialog“ blockieren.
Stilles Feuer (Endometritis): Chronische und nicht wahrnehmbare Entzündungsprozesse, die die Gebärmutter unbewohnbar machen.
Frühe Abstoßung: Aggressive Reaktionen, die zu einem Schwangerschaftsverlust führen, noch bevor die Schwangerschaft klinisch nachweisbar ist.
Autoimmunfaktoren: Vorbestehende Störungen, bei denen der Körper darauf programmiert ist, eigenes Gewebe anzugreifen, was das Risiko einer Fehlgeburt erhöht.
Jüngste Studien untersuchen den Zusammenhang zwischen Entzündungsmarkern und wiederholtem Implantationsversagen. Obwohl noch nicht schlüssig, deuten sie darauf hin, dass bestimmte immunologische Profile die Erfolgsaussichten selbst bei Techniken der assistierten Reproduktion drastisch reduzieren.
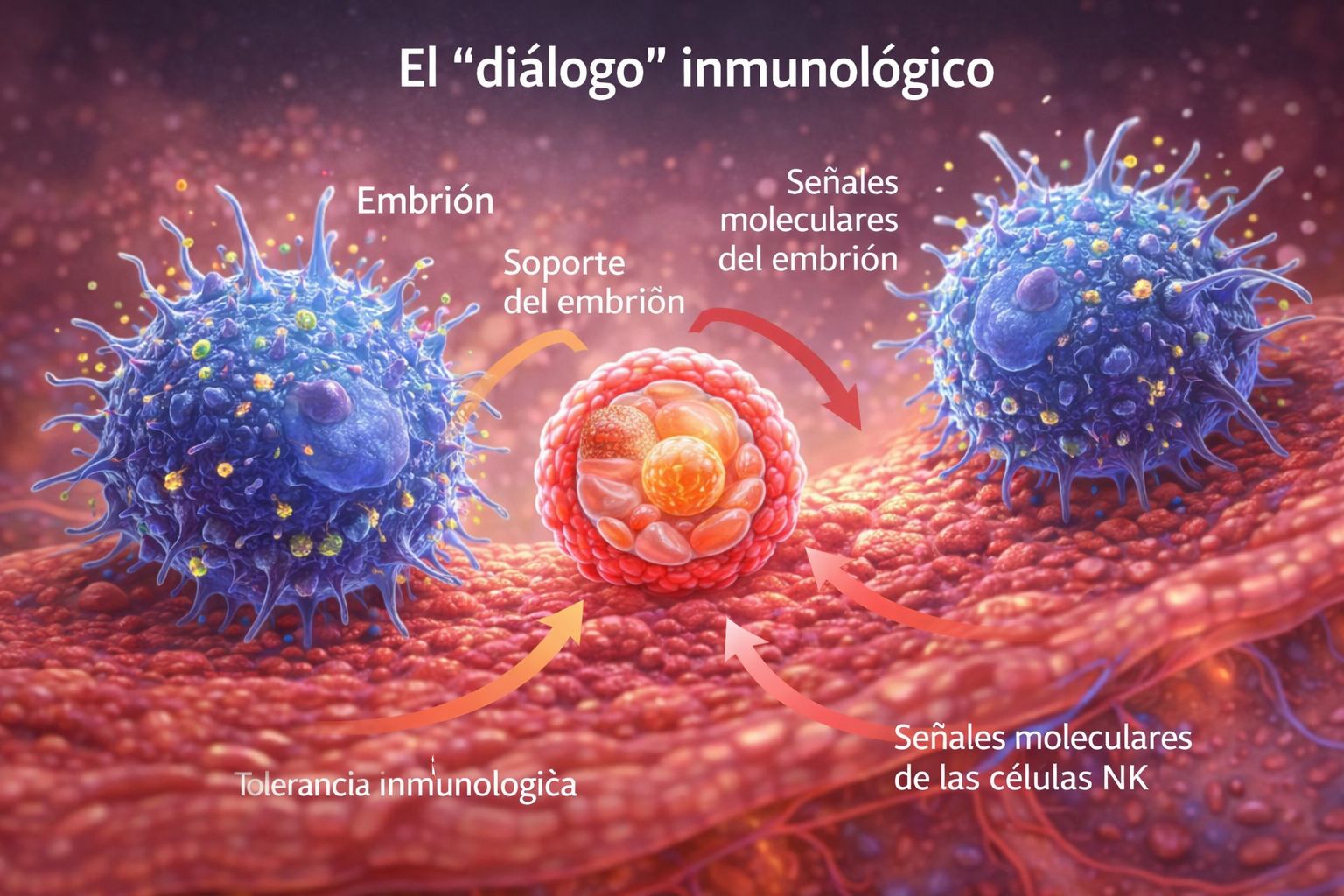
Die Wächterinnen der Gebärmutter: Uterine NK-Zellen
Eine der relevantesten Entdeckungen ist die Rolle der uterinen Natürlichen Killerzellen (uNK). Im Gegensatz zu ihren Verwandten im Blutkreislauf, deren Aufgabe die Eliminierung infizierter Zellen oder Tumorzellen ist, haben die uNK-Zellen in der Gebärmutter eine konstruktive Mission:
Sie regulieren die Tiefe der Implantation.
Sie steuern den Umbau der mütterlichen Blutgefäße zur Ernährung des Embryos.
Sie unterstützen die frühe Entwicklung der Plazenta.
Im frühen Endometrium können diese Zellen bis zu 70 % der lokalen Immunzellen ausmachen, was bestätigt, dass sie die entscheidenden Architekten der uterinen Umgebung sind. Ein Ungleichgewicht in ihrer Aktivität — sei es durch übermäßige Aggression oder mangelnde Unterstützung — kann über die Zukunft der Schwangerschaft entscheiden.
Die Zukunft der Reproduktionsmedizin: Zwischen Hoffnung und Vorsicht
Sollte sich diese Hypothese festigen, stehen wir vor einem Paradigmenwechsel, der Folgendes umfassen würde:
Präzisionsdiagnostik: Integration immunologischer Profile in Routineuntersuchungen.
Gezielte Immunmodulation: Therapien, die die uterine Toleranz fördern, ohne die allgemeine Abwehr zu unterdrücken.
Ganzheitliche Ansätze: Behandlung systemischer Entzündungen als Teil des Fruchtbarkeitsprotokolls.
Dennoch mahnt die wissenschaftliche Gemeinschaft zur Vorsicht. Das Feld ist komplex und zuweilen kontrovers. Vielen vorgeschlagenen Behandlungen fehlt es noch an solider klinischer Evidenz, und Fachgesellschaften wie die ESHRE oder ASRM weisen auf die Notwendigkeit weiterer groß angelegter Studien hin, bevor diese Therapien in der Routinepraxis standardisiert werden.

Hin zu einer neuen reproduktiven Souveränität
Über Jahrzehnte war Fruchtbarkeit eine Frage der Mechanik und Chemie. Die Immunologie fügt nun eine tiefere, fast philosophische Dimension hinzu: Fruchtbarkeit ist kein statischer Zustand, sondern ein dynamisches Gleichgewicht.
Die Herausforderung des 21. Jahrhunderts besteht nicht nur darin, Hormone zu stimulieren oder Labortechniken zu perfektionieren, sondern das Dreiergespann aus Immunität, Entzündung und Fortpflanzung zu verstehen. Die offene Frage ist ebenso einfach wie tiefgründig: Wie viele Fälle von Unfruchtbarkeit bleiben unsichtbar, weil wir noch nicht gelernt haben, auf die immunologische Sprache des Körpers zu hören?
Wissenschaftliche Belege und Quellen:
National Institutes of Health (NIH): [www.nih.gov]
Nature / The Lancet: Studien zu uNK-Zellen und Entzündungsmarkern.
ESHRE / ASRM: Konsensdokumente zur idiopathischen Sterilität.
#ImmunologischeUnfruchtbarkeit #Reproduktionsmedizin #Frauengesundheit #MedizinischeInnovation #HoyLunes #EhabSoltan
Diese Informationen dienen ausschließlich Informationszwecken. Für eine medizinische Beratung oder Diagnose wenden Sie sich bitte an einen Experten.